Actividad 1: ¿Qué son los hidrocarburos?
Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno. Consisten en un armazón de carbono al que se unen átomos de hidrógeno. Forman el esqueleto de la materia orgánica. También están divididos en abiertas y ramificadas.
Actividad 2: Realiza una clasificación de los hidrocarburos en función del tipo de enlace que presentan. Describe las propiedades más importantes de cada uno.
Según la estructura de los enlaces entre los átomos de carbono, se clasifican en:
- Hidrocarburos acíclicos, alifáticos, unalifáticos, o de cadena abierta: estos a su vez se dividen en:
- Hidrocarburos saturados (alcanos o parafinas), que no tienen enlaces dobles, triples, ni aromáticos, sólo múltiples enlaces individuales, y de cadena.
- Hidrocarburos no saturados o insaturados, que tienen uno o más enlaces dobles (alquenos u olefinas) o triples (alquinos o acetilénicos) entre sus átomos de carbono.
- Hidrocarburos cíclicos, hidrocarburos de cadena cerrada que a su vez se subdividen en:
- Cicloalcanos, que tienen cadenas cerradas de 3, 4, 5, 6, 7 y 8 moléculas de carbono saturados o no saturados.
- Hidrocarburos aromáticos, no saturados, que poseen al menos un anillo aromático además de otros tipos de enlaces.
Los hidrocarburos extraídos directamente de formaciones geológicas en estado líquido se conocen comúnmente con el nombre de petróleo, mientras que los que se encuentran en estado gaseoso se les conoce como gas natural. La explotación comercial de los hidrocarburos constituye una actividad económica de primera importancia, pues forman parte de los principales combustibles fósiles (petróleo y gas natural), así como de todo tipo de plásticos, ceras y lubricantes.
Actividad 3: Realiza los siguientes ejercicios de formulación
Alcanos - Señala el nombre correcto para estos compuestos:\
NOTA: Si no se ven las imagenes dar clic derecho y seleccinar "Ver imagen".
1.
| 2.
|
3.
| 4.
|
5.
| 6.
|
7. Alcano lineal de 10 carbonos
| 8.
|
9. Alcano lineal de 11 carbonos
| 10.
|
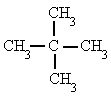
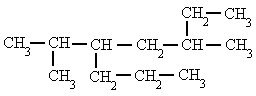
Alcanos - Señala el nombre correcto para estos compuestos
| 1. Metil-propano | 2. Metil-butano |
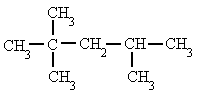
| 3. Dimetil-propano | 4. 2-metil-pentano |
5. 2,3-dimetil-butano | 6. 3-metil-hexano |
| 7. 5-isopropil-3-metil-octano | 8. 4-etil-2,2,4-trimetil-hexano |
| 9. 2,2,4-trimetil-pentano | 10. 2,2,7,7-tetrametil-nonano |
Alquenos- Señala el nombre correcto para estos compuestos:
| 1. 1-buteno | 2. 2-penteno |
| 3. 2,3-butadieno | 4. 1,3,5-hexatrieno |
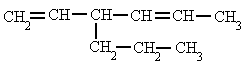
| 5. 4-metil-1-penteno | 6. 2,5-dimetil-1,3-heptadieno |
| 7. 2-etil-5,5-dimetil-1,3-hexadieno | 8. 3-propil-1,4-hexadieno |
| 9. 3-etil-1,3-pentadieno | 10.
|
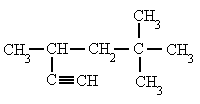
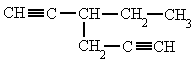
Alquinos – Señala el nombre correcto para estos compuestos:
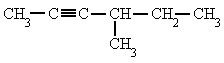
| 1. 1-pentino | 2. 4-metil-2-hexino |
| 3. 6-metil-3-propil-1,4-heptadiíno | 4. 3,5,5-trimetil-1-hexino |
| 5. 3-etil-1,5-hexadiíno | 6. 2,7-dimetil-3,5-nonadiíno |
| 7. 1-buten-3-ino | 8. 1,3-hexadien-5-ino |
| 9. 3-metil-1-hexen-5-ino | 10. 3-penten-1-ino |
Actividad 4: ¿Dé que están formados el petróleo y el gas natural? Realiza un pequeño artículo donde se recojan las características de ambas sustancias, su uso, obtención y consecuencias para el medio ambiente.
El petróleo y el gas natural
El petróleo es un líquido formado por una mezcla de hidrocarburos. En las refinerías se separan del petróleo distintos componentes como gasolina, gasoil, fuel-oil y asfaltos, que son usados como combustibles.
El gas natural está formado por un pequeño grupo de hidrocarburos: fundamentalmente metano con una pequeña cantidad de propano y butano. El propano y el butano se separan del metano y se usan como combustible para cocinar y calentar, distribuidos en bombonas. El metano se distribuye normalmente por conducciones de gas a presión.
En 1990 se obtenía del petróleo el 38,6% de la energía comercial del mundo, en 1974 llegó a representar el 47,4%.
Formación
El petróleo y el gas natural se forman cuando grandes cantidades de microorganismos acuáticos mueren y son enterrados entre los sedimentos del fondo de estuarios y pantanos
El petróleo y el gas, al ser menos densos que la roca, tienden a ascender hasta quedar atrapados debajo de rocas impermeables.
Tipos de crudo
La composición de los crudos es muy variable dependiendo del lugar en el que se han formado. No solo se distinguen unos crudos de otros por sus diferentes proporciones en las distintas fracciones de hidrocarburos, sino también porque tienen distintas proporciones de azufre, nitrógeno y de las pequeñas cantidades de diversos metales, que tienen mucha importancia desde el punto de vista de la contaminación.
Reservas de petróleo y de gas natural
Se puede encontrar petróleo y gas natural en todos los continentes distribuidos de forma muy irregular.
Es muy difícil estimar para cuantos años tenemos petróleo y gas natural. Es difícil hacer este cálculo porque depende de muchas variables desconocidas. No sabemos cuantos depósitos nuevos se van a descubrir. Tampoco cual va a ser el ritmo de consumo.
Otro importante problema relacionado con el petróleo es que se consume mayoritariamente en regiones donde no se produce.
Consumo de petróleo
El consumo mundial de petróleo fue creciendo hasta alcanzar su máximo en 1978 año en el que se explotaron algo más de 3000 millones de toneladas. Después el consumo disminuyó hasta el año 1982 y desde entonces ha ido aumentando pero todavía sin llegar a las cifras de 1978. El consumo medio en el mundo, por habitante y año en 1993 era de unas 0,6 toneladas
Problemas ambientales en el uso del petróleo y el gas natural
Estos combustibles causan contaminación tanto al usarlos como al producirlos y transportarlos.
Uno de los problemas más estudiados en la actualidad es el que surge de la inmensa cantidad de CO2 que estamos emitiendo a la atmósfera al quemar los combustibles fósiles. Este gas tiene un importante efecto invernadero y se podría estar provocando un calentamiento global de todo el planeta con cambios en el clima que podrían ser catastróficos.
Otro impacto negativo es la lluvia ácida, en este caso no tanto por la producción de óxidos de azufre, como en el caso del carbón, sino sobre todo por la producción de óxidos de nitrógeno.



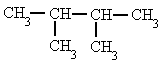
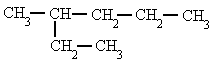


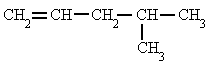
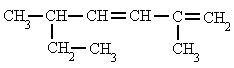
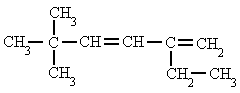
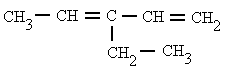
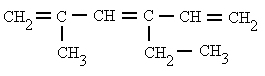
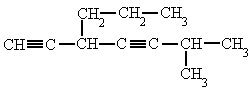
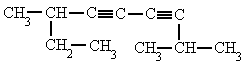
No hay comentarios:
Publicar un comentario